📚Ici vous trouverez tout QCM, contrôles et examens de chimie générale S1 avec corrigés PDF – SVTU et BCG. 1ère année Licence Biologie (Sciences de la Vie, de la Terre et de l’Univers)
Vous pouvez télécharger et passer des examens en ligne avec nous.
N’hésitez pas de communiquer avec les autres étudiants via la section les commentaires.
Examens à Télécharger en PDF
Examens scannés: Examens corrigés de chimie générale s1 pdf semestre 1 à télécharger
Examens de chimie générale PDF Scanné 1
Examens de chimie générale PDF Scanné 2
Examens de chimie générale PDF Scanné 3
Examens de chimie générale PDF Scanné 4
Examens PDF 5
Examens PDF 6
Examens PDF 7
Examens PDF 8
Examens PDF 9
Examens PDF 10
Examens PDF 11
Examens PDF 12
Examens PDF 13
Examens qcm atomistique PDF 14
Examens qcm structure électronique atome PDF 15
💳💥 Examens PREMIUM de chimie générale S1 Avec Solutions PDF
Examens de chimie générale S1
Contrôle d’atomistique
Durée 1h 30mn
N.B : Le tableau périodique des éléments n’est pas autorisé
Exercice I
1) Le Gallium (Z =31) existe sous forme de deux isotopes 69Ga et 71Ga avec les proportions respectives de 64% et 36%, calculer sa masse molaire.
2) Calculer le nombre d’atome contenu dans 927 mg de Gallium.
3) Lequel des échantillons suivants contient le plus de Gallium : 5g de Ga, 0,05 atome-gramme de Ga ou 5.1022 atomes de Ga. (N = 6,02.1023).
Exercice II
1) Le spectre de l’ion hydrogenoide 7N6+ comporte une raie de longueur d’onde 223,3 Ǻ, appartenant à la série de Paschen.
a) Calculer son énergie en ev.
b) A quelle transition électronique de m vers n cette raie est associée ?
2) Toujours dans le cas de l’ion 7N6+ déterminer :
a) L’énergie minimale d’excitation.
b) La fréquence correspondante à une transition de l’état fondamental au 2ème état excité.
c) L’énergie nécessaire pour ioniser cet ion à partir de son état fondamental.
d) L’expression de l’équation de Schrödinger.
On donne : c = 3 108 m/s, h = 6,62 10-34 j.s, RH = 1,0967 107 m-1 et 1 ev = 1,6 10-19 j.
Exercice III
Le vanadium (Z=23) peut donner les ions V2+, V3+, V4+et V5+ en perdant respectivement deux, trois, quatre et cinq électrons.
1) Donner la configuration électronique du vanadium et de ses quatre ions.
2) Donner les valeurs des quatre nombres quantiques des électrons célibataires de V3+.
3) A quelle groupe et à quelle période appartient le vanadium.
4) Déterminer la configuration électronique et le numéro atomique Z des éléments qui appartiennent à la même période que le vanadium et qui possèdent deux électrons célibataires.
5) Calculer la charge Z* effective pour chaque électron de l’ion V2+.
6) En utilisant les règles de Slater, calculer l’énergie d’ionisation de l’ion V4+ en ion V5+
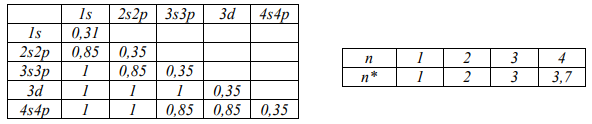
-Les valeurs des coefficients d’écran et celles de n*.
Autres Examens en Photos







Bien qualitatif
Merci beaucoup Jean
Merci Pierre.